メラトニンアゴニストの化学式を図2に示す。TIK-301(=β-メチル-6-chloromelatonin)を除いて、これらの化合物は非インドール構造を持つ。ラメルテオン(ロゼレム、TAK-375、武田薬品が開発)はFDAによって米国で不眠症の使用が承認されている。ラメルテオン代謝産物であるM-IIもメラトニン受容体への作用を持つ。アゴメラチン(Valdoxan、S20098、セルヴィエ社が開発)はヨーロッパで成人の大うつ病の治療のために使用されている。これらの合成薬物やメラトニン徐放錠(Circadin)は55歳以上の不眠症で承認されている。他は前臨床段階か治験中である。MT1やMT2受容体への親和性を表3に示す(注;よく使用される解離常数とは違いlogの値に変換したPKi値が提示されており、数字が大きい方が親和性が高いことになる)。天然のホルモンであるメラトニンよりもMT1やMT2受容体に対しては親和性が幾分高めのようである。化合物はいずれも2つの受容体に対して選択的には作用しないが、MT1とMT2では、親和性がかなり異なるUCM765やUCM924のような化合物もある。この受容体への親和性の差が疾患の治療に応用できるかどうかはまだ研究されていない。
メラトニンの半減期は20~30分(最大でも約45分)と非常に短いため臨床的に使用する上での大きな障壁となる。この半減期が短いという問題に対する解決策としてCircadinなどのメラトニンの徐放製剤が発売され、メラトニンよりも長い半減期をもつ合成薬も開発されている。ラメルテオンは急速に消化管で吸収され(約84%の吸収率)、半減期は1~2時間である。メラトニン作動薬の中では、ラメルテオンは、肝臓のチトクロームPで代謝されるが、メラトニンとは異なり、主にCYP1A2、CYP2C、CYP3Aによって代謝される。ラメルテオンの代謝物の中でも、M-IIはアゴニストとして作用し、ラメルテオンと比較してMT1やMT2には10%の効力を持つ。ラメルテオンよりも20~100倍血中濃度が高いため、親和性が低いにも係らず、M-IIはラメルテオンの機能に関連している。また、M-IIの半減期はラメルテオンよりも2~5時間も長い。
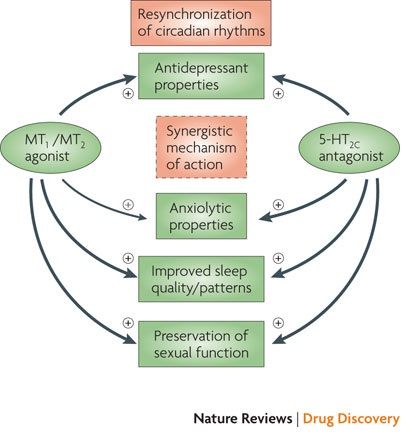
アゴメラチンの半減期は1~2時間であり、受容体への親和性はメラトニンよりもいくぶん強めである。メラトニンやラメルテオンににはないセロトニン受容体5-HT2Cのアンタゴニスト作用を有する。5-HT2Cへの作用は、概日リズム障害やある種のうつ病のサブタイプに有効である概日リズムの調整といったメラトニンの作用と区別されなければならない。アゴメラチン抗うつ作用は5-HT2C介する作用と思われているが、最近では、メラトニンと5-HT2Cの相乗作用や相互作用がアゴメラチンの抗うつ薬としての作用であろうと想定されている。
メラトニンアゴニスト+セロトニンアンタゴニストの組み合わせを有する薬剤には、TIK-301もある。この薬物はアゴメラチンよりも5-HT2C受容体を一層強力に阻害し、5-HT2B受容体も阻害する。TIK-301もアゴメラチンに匹敵するような抗うつ作用を有するものと思われる。合成メラトニン作動薬は主に催眠効果に焦点を当てらて研究されている。化学構造が異なるためCYPアイソザイムによるメラトニンの主要な異化であるヒドロキシル化を防止する。半減期は長くなってもいいはずであるが、TIK-301の半減期は1時間である。TIK-301は、FDAによるオーファンドラッグ(希少疾病用医薬品)の指定を受け盲患者における睡眠障害の治療に使用されている。
Tasimelteonが既に臨床試験されている。睡眠剤としてであるが、前臨床試験では抗うつ効果が確かめらている。しかし、5-HT2C受容体への作用は確認されていない。tasimelteonの半減期は長く。サルやラットでは、2時間(1~3時間)と報告されている。
他の合成メラトニン作動薬の睡眠に関する前臨床データは存在するが、臨床上の薬物動態のデータはまだ少ない。GR196429とAH-017はラットのメラトニンの振幅を大きくすることが報告された。他の合成メラトニン作動薬によりも逸脱した位相をリセットする能力に優れているかを検証する必要がある。MT2受容体への親和性が高いAH-017、UCM765、UCM924の作用をさらに調査する必要がある。UCM765はMT2受容体を介して網状視床ニューロンの発火を刺激しノンレム睡眠を増やすことが示された。これらの化合物にはMT2受容体を介した疾患の治療効果が存在するかもしれない。UCM924はフッ素原子を取り付けることによってUCM765のヒドロキシル化部位を遮断し、UCM765の0の部位における脱メチル化を防止するために臭素を付加することで半減期を長くするように設計されている。。図や表に提示されていないが、NEU-P1という新しいメラトニンアゴニストは、high-fat/high-sucrose-fedラットにおける体重増加を抑制しインスリン感受性を改善することが報告されており注目を集めている。
短期作用に基づいた治療のためのオプション
時間生物学的への戦略についての概略を説明する。
短時間作用型のみのメラトニンが必要な疾患と、不十分な夜間のメラトニンレベルを補うような補完療法的な使用が必要な疾患とを区別することが重要である。最初のケースでは、治療としては半減期が短い天然ホルモンであるメラトニンで十分である。特に、入眠困難の場合には十分である。メラトニンは既に0.1~0.3mgの低用量(即時放出製剤)で入眠までの時間を短くした。しかし、睡眠維持への効果は、この用量では殆どない。入眠潜時の有意な減少が全ての合成メラトニンアゴニストで観察されている。しかし、これらの薬剤の推奨用量はメラトニンよりも高い受容体親和性にもかかわらず、ラメルテオンの4mgと8 mg、アゴメラチンの25mgと、かなりの高用量となっている。従って、合成薬物は入眠改善以外の作用もある。脳波所見ではラメルテオンは徐波睡眠やレム睡眠を増加させた。ラメルテオンはメラトニンよりも睡眠維持効果が期待できる。自然なホルモンであるメラトニンは忍容性や生理学的な代謝に関しては好ましいプロフィールを有する。MT1 / MT2を介さないような効果は合成薬剤には存在しないだろう(フリーラジカルスカベンジャーとしての作用など)。なお、化学式からはラメルテオンにはメラトニンのような抗酸化作用はないと考えられている(=メラトニン以外はアンチエイジングのような効果はない)。
位相をシフトさせるなどの時間生物学的な観点からは、ショートアクションでも十分である。概日リズムの発振器のリセットは、概日リズムが乱れている場合に必要となる。概日リズムの乱れは、(1)夜の光や子午線を越えるような飛行、(2)体内時計が環境の時間サイクルに少ししか同調していない、(3)マルチ発振器システムの位相の逸脱や非同調によって生じる。(2)は、年齢や疾患が起因するメラトニン分泌が低下するような条件の下で、発振器の振動がフラットになることで生じる可能性がある。このため、概日リズムの振幅を高めることができる薬剤に関心が持たれている。外部の同調器(日照時間など)と内部の発振器と間の脱同調や異常な位相関係、並列発振器同士の脱同調や異常な位相関係といった同調性の問題という現象は体系的に調査されていないが、この現象は双極性障害と季節性感情障害も含めた物理的および精神的なフィットネスの障害に関与しているものと思わる。概日リズムの誤動作が気分障害に関与しているのであれば、メラトニンやメラトニン作動薬は概日リズムを再調整すること気分障害の症状を改善できるものと思われる(ラメルテオンではMT2を介した位相シフトを促進するという概日ペースメーカーへの作用が確認されている。)
ここでアゴメラチンやTIK-301のようなセロトニン受容体を介した直接的な抗うつ効果を混同しないことが重要である。合成メラトニン薬による治療は、概日リズムに有益であることが予想されるが、メラトニンよりもMT受容体への親和性が高いことや半減期が長いことが優れた有効性を期待できる訳ではない。メラトニンのような短時間作用型の時間生物物質は、位相を同調させる能力を有するが、概日リズムの発振器は感受性が広くノンパラメトリック・リセッッティングと呼ばれる。例えば、シンクロナイザー(メラトニン)の絶対的なレベルよりも相対的な変化という刺激が同調因子としての決定因子となる。
位相をリセットする治療では時間生物学的な基本的な規則を考慮する必要がある。既に解説したようにリセット信号は、それぞれのPRC信号に応じて作動している。ヒトでは、リセット信号としてのPRCを機能させる上で、メラトニンが投与されるタイミングが最も重要となる。概日リズムのサイクルの中で、適切で十分に感受性を有する位相でメラトニンが投与された場合に限ってメラトニンによる概日リズムの再調整が達成される。シンクロナイザー(外界の光の変化)との乏しいカップリングのために概日リズムが同調されていない場合は、発振器が所望の位相に到達するまでに数日以上かかることがある。これらの時間生物学的な基礎を無視した方法はメラトニンの投与が無効であるという誤った結論につながることになる。
メラトニンや合成メラトニンが概日リズムをリセットする唯一の手段ではない。SCNとの神経接続が障害されていない場合ではあるが、長時間の青色の光刺激(または緑色光)によっても概日リズムはリセットされる。光療法は概日リズムのリセットのオプションの一つになりうる。ある個体では、光刺激とメラトニンの組み合わせが概日リズムのリセットにおいて好ましく、かつ、有利であろう。しかし、SCNの光信号の受容が障害されている条件下では、メラトニンのみしか効果がない場合がある。
(概日リズムリセット装置。↓)
(概日リズムリセット装置。↓)
代替療法の限界
短時間しか作用しないメラトニンの使用は補充療法としては区別される必要がある。メラトニンの使用は、高齢者やメラトニンのレベルが減少する様々な疾患の患者には好ましいであろう(表1)。しかし、短い半減期のために、メラトニンの即時放出製剤では、十分な補完を可能にすることはできない。
従って、合成アゴニストや徐放性のメラトニンの方が優れていると推定される。メラトニン自体は忍容性に非常に優れているため、メラトニンの徐放製剤が最初に試されることになろう。合成薬の中では、ラメルテオンがFDAによって既に承認されているので、アメリカでは選択肢の1つかもしれない。ヨーロッパでライセンスされているアゴメラチンは比較的良好な結果が得られている。しかし、いずれの薬剤も使用が限定されている。例えば、メラトニンの徐放製剤であるCircadinは55歳以上のみの適応に限るといったように。従って、全ての疾患に使用できる訳ではない。睡眠導入や時間生物学的な効果からはアゴメラチン、ラメルテオン、メラトニンが推奨されるが、適応症に限りがある。
睡眠の維持や睡眠の質に関してもこれらの薬物が有効であると報告されているが、統計的なデータでは睡眠障害の改善度は中等度である。慢性的な不眠症を有する高齢の患者では、睡眠の維持効果においてはラメルテオンは個人差が大きいことが分かっている(睡眠維持のメカニズムはメラトニンよりも下流の機能が関与しているため、睡眠の維持効果は期待できないであろう。これは全てのメラトニン作動薬に当てはまることである)。統計的に睡眠時間や睡眠効率の増加が実証されているが、これらの知見は夜間の睡眠の持続的で完全な改善を意味するものではない。同じことが他のメラトニン作動薬物についても言える。睡眠開始や睡眠効率に関しては適度に良好な結果を有するが、メラトニンが欠乏するような場合においては、補充療法としてはメラトニン作動薬物のいずれでも十分な睡眠の改善は達成されていない。さらに、50mgや100mgのようなメラトニンよりもはるかに高用量で補充が可能になるかどうかも試験されていない。メラトニンの徐放製剤であるCircadinの標準用量はわずか2mgである。忍容性および有害性の面では、メラトニンの投与量は合成メラトニン作動薬物よりも懸念が少ない。しかし、300mgのメラトニンを経口で2年間ALSの患者に投与したが安全であることが報告されている。
うつ病におけるアゴメラチンの使用に関しては、うつ症状が概日リズムの機能不全に基づくものか、他の理由に基づくものかを区別する必要がある。概日リズムの機能不全のケースでは、位相調整という時間生物学的観点からは、アゴメラチンの有効性は、MT受容体親和性を有する他のものと区別することができない。大うつ病では、うつ症状は主に概日リズムに起因しているのではなく、うつ症状の改善は5-HT2cの阻害作用に起因しているか、あるいは、MT1 / MT 2と5-HT2Cの相互作用によるものであろう。しかし、これらのプロパティは、古典的な抗うつ薬とは異なる。このため、何人かの研究者は、既存の抗うつ剤の効果が不十分な大うつ病性障害に対するアゴメラチンの有効性を検討した。アゴメラチンでは作用機序を区別することが必要である。アゴメラチンの利点は優れた抗うつ効果にあるのではなく、睡眠の改善作用と抗うつ効果の組み合わせであることが分かった。睡眠障害は、古典的な抗うつ薬でしばしば生じるため、この二重の作用は重要である。
メラトニン作動薬の制限が薬物相互作用に起因することがある。CYPアイソフォームを阻害する他の薬物の存在下で、高濃度を呈することによる。例えば、ラメルテオンは主にCYP1A2、CYP2C9、CYP3A4によって代謝され、アゴメラチンはCYP1A、CYP1A2、CYP2C9に代謝され、tasimelteonはCYP1A1、CYP1A2、CYP2D6、CYP2C9 によって代謝される。従ってCYPを阻害するようなフルボキサミン、シプロフロキサシン、メキシレチン(抗不整脈剤)、ノルフロキサシン、azileuton、フルコナゾール(抗真菌剤)、ケトコナゾール(抗真菌剤)などの薬剤との併用は避けなければならない。メラトニンの場合には、CYP阻害によって引き起こされる血中濃度は上昇は重篤な副作用は呈さずに、比較的無害である。にも係らず、自己免疫疾患では全てのメラトニン作動薬ではWillisらによって警告がなされている。なぜならば、メラトニンには免疫調整作用があり、特に、パーキンソン病、小児、妊娠中での使用は禁忌であると警告されている。メラトニンは、子供や妊婦に使用されることもあるが、利益と危険性を同時に考慮する必要がある。承認された合成アゴニストに関しては、肝、腎機能障害、アルコールとの併用、高脂肪食との併用も禁忌として記載されている。
全ての臨床試験においてメラトニンアゴニストは忍容性に優れていたが、長期間の使用では副作用に注意する必要がある。ラメルテオンの長期使用時の安全性を述べた論文も多いが、多くは主に吐き気や頭痛といった軽度の有害事象にしか触れていない。さらに、肝臓機能への影響、残留性(翌日への持越し?)、リバウンド的な不眠症、6~12ヶ月間使用後の離脱症状や依存性、などといった有害事象はないと報告されている。しかし、長期使用時の変異原性や発癌性が排除されている訳ではない。変異原性はないと発売元はデータで示しているが、それはラメルテオンの場合だけであり、ラメルテオンの主代謝物であるM-IIをも考慮する必要がある。しかも調べられたラメルテオンの濃度はM-IIの3倍までの濃度のデータである。M-IIはラメルテオンよりも20~100倍もの高濃度になるため体内に蓄積すると思われるが、M-IIによる肝毒性、小核形成(核の形が変化し発癌につながる変化が)、変異原性をも考慮する必要があるが、M-IIによる影響はまだ何も調べられていない。なお、ラメルテオンでは小核形成がラットの肺で認められている。、
アゴメラチンの場合にも毒性の懸念は存在するであろうが、短期間の使用では忍容性は良好である。しかし、ナフタレン化合物であるため、CYP関連の肝臓への影響や発癌性を含めた長期の毒性を調べる必要がある。CYP依存性代謝に関しては、薬物相互作用の問題としてではなく、ナフタレン物質の基本的な問題である毒性を有する代謝産物の形成が問題になろう。アゴメラチンの25mg/日という比較的高容量の推奨用量が考慮されねばならない。アゴメラチンの肝毒性のリスクが最近になって示された。さらに、動物実験で観察された高用量における発癌性は警告として解釈すべきである。メラトニン作動薬では長期的な安全性に関しては代謝物のプロパティをも考慮する必要がある。この点でラメルテオンはメラトニンよりも必ずしも優れているとは言えないかもしれない。
(特に、ラメルテオンでは、メラトニン製剤よりも半減期が長く高用量が使用され、MT受容体への親和性も高いため、長期使用ではMT受容体のダウンレギュレーションを引き起こす可能性がある。MT受容体のダウンレギュレーションが免疫系などの末梢組織においてはどのような影響を及ぼすかはまだ不明である。)
(論文終わり)
メラトニンは日本の薬局には売っておらず、アマゾンなどで購入するしかない。アマゾンでは簡単に購入できる。私は50歳を過ぎており、認知症になりたくないので既にメラトニン徐放剤を内服している。効果の程は20年後くらいに分かることであろう(もう、手遅れかもしれないが^^;)。
(論文終わり)
メラトニンは日本の薬局には売っておらず、アマゾンなどで購入するしかない。アマゾンでは簡単に購入できる。私は50歳を過ぎており、認知症になりたくないので既にメラトニン徐放剤を内服している。効果の程は20年後くらいに分かることであろう(もう、手遅れかもしれないが^^;)。
http://www.amazon.co.jp/s/?ie=UTF8&keywords=%E3%83%A1%E3%83%A9%E3%83%88%E3%83%8B%E3%83%B3+%E3%82%B5%E3%83%97%E3%83%AA%E3%83%A1%E3%83%B3%E3%83%88&tag=googhydr-22&index=hpc&jp-ad-ap=0&hvadid=23873272625&hvpos=1t1&hvexid=&hvnetw=g&hvrand=944504331508848955&hvpone=&hvptwo=&hvqmt=b&hvdev=c&ref=pd_sl_9ark7bpfod_b
